4차산업혁명위서 발전전략 확정...2022년까지 건강수명 76세·일자리 18만명 달성
[라포르시안] 헬스케어 빅데이터 생산·관리 시범체계가 운영되고 인공지능 기반 신약개발이 추진된다. 헬스케어 산업 혁신 생태계도 조성된다.
보건복지부는 10일 광화문 회의실에서 관계부처와 합동으로 대통령 직속 4차산업혁명위원회 제9차 회의를 열고 이런 내용을 담은 '4차 산업혁명 기반 헬스케어 발전전략'을 확정했다.
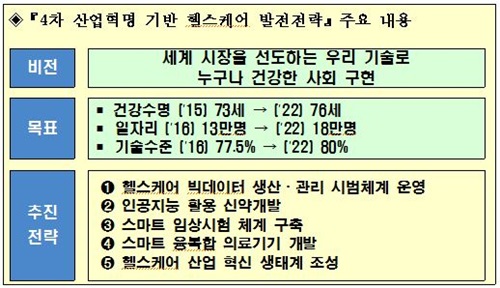
헬스케어 발전전략은 '세계 시장을 선도하는 우리 기술로 누구나 건강한 사회 구현'을 비전으로 설정하고 2022년까지 건강수명 76세, 일자리 18만명, 기술수준 80% 달성을 목표로 삼았다.
중점 추진 과제로 ▲헬스케어 빅데이터 생산·관리 시범체계 운영 ▲인공지능 활용 신약개발 ▲스마트 임상시험 체계 구축 ▲스마트 융복합 의료기기 개발 ▲△헬스케어 산업 혁신 생태계 조성을 도출하고 세부 추진전략을 마련헀다.
주요 내용을 보면 우선 헬스케어 빅데이터 생산·관리 시범체계를 운영한다.
일반인, 암생존자 등 300명의 건강·의료·유전체 데이터를 통합·분석해 헬스케어 빅데이터 활용경험을 축적하고 내년부터 2021년까지 표준개발에 활용하기 위한 '헬스케어 빅데이터 쇼케이스 사업'을 추진한다.
인공지능을 신약개발에 활용해 신약개발을 위한 기간·비용을 단축하는 등 국가적 신약개발 역량을 높인다.
2021년까지 인공지능 신약개발 기반(플랫폼) 구축사업을 통해 후보 물질 발굴, 전임상시험, 스마트 약물감시 등 신약개발 전 단계에 활용가능한 단계별 인공지능 플랫폼을 개발할 계획이다.
인공지능 플랫폼을 활용하고 관련 빅데이터를 수집·관리할 수 있는 신약개발 전문인력 양성을 병행하고 인공지능 플랫폼을 활용해 직접 연구를 수행할 제약사 내부인력 전문화 교육을 추진한다.
스마트 임상시험 구축 사업을 통해 신약 개발 지원체계를 고도화한다.
차세대 임상시험관리시스템(CTMS) 개발을 통해 임상시험 센터별 각기 다른 관리시스템을 2021년까지 통일된 형식으로 전환하고, 차세대 임상시험 신기술 개발을 추진해 임상시험 효율성 및 품질을 높이기로 했다.
다기관 임상시험 수행 시 IRB(기관생명윤리위원회) 심사 상호인증‘ 제도를 2021년까지 시범 운영하고 혁신형 제약기업의 신약 개발 승인·허가 기간을 단축하는 등 임상시험 단계별 제도개선을 추진한다.
스마트 융복합 의료기기 개발을 위해 연구개발 지원, 수요창출, 규제개선 등 전주기 지원 체계를 구축한다.
이를 위해 빅데이터, AI, 3D프린팅 등 신개념 의료기기 개발을 지원하기 위한 범부처 연구개발(R&D) 사업을 추진한다.
병원 수요를 반영한 구매조건부 R&D 프로그램 도입, 국내 대형병원 시범사용 등 국산 융복합 의료기기 판로 확대를 지원한다.
신의료기술평가 제도를 개선해 혁신의료기술의 잠재가치를 평가하는 별도의 평가체계를 구축하고 체외진단기기 신의료기술평가는 내년 1월부터 사후평가방식으로 전환한다.
기술확보에서 창업, 성장, 투자회수를 거쳐 재투자까지 유기적으로 연계되는 역동적인 헬스케어산업 생태계 조성도 추진된다.
지역 바이오헬스 클러스터와 지방거점 병원을 연계하고 병원·기업 간 공동연구 확산을 위한 개방형 실험실 구축을 지원해 개방형 혁신을 가속화할 예정이다.
기초과학·정보기술(IT) 등 타 학문 지식·연구방법론을 체득한 융합형 의사과학자를 양성하고 MD·Ph.D 공동연구 지원을 확대해 헬스케어 혁신을 선도할 현장·연구 전문인력을 양성한다.
보건산업 혁신 창업센터를 통해 창업기업 밀착 지원체계를 구축하고 '보건산업 창업기업 실태조사'를 정례화해 정책개발의 효과성을 높일 계획이다.
복지부 임숙영 보건산업정책과장은 "내년도 신규 사업과 제도 개선 확정 과제는 일정에 따라 추진하고 추가적인 논의를 거쳐 계획 구체화·신규 사업 개발이 필요한 과제는 소관 부처 검토를 거쳐 계속 추진할 예정"이라고 밝혔다.

