[라포르시안] 의료 인공지능(AI)기업 뷰노(대표 이예하)는 자사 AI 기반 심정지 예측 의료기기 ‘뷰노메드 딥카스’(VUNO Med–DeepCARS)가 국내 의료AI 업계 최초로 미국 FDA로부터 혁신의료기기로 지정됐다고 8일 밝혔다. 뷰노메드 딥카스는 이번 혁신의료기기 지정으로 미국 FDA 승인 시점을 앞당길 수 있게 됐다.
미국 FDA의 혁신의료기기 지정은 환자에게 효과적으로 최선의 이익을 제공하는 획기적 의료기술이 보다 신속하게 시장에 진입할 수 있도록 돕기 위해 마련된 제도다. 혁신의료기기로 지정된 의료기기는 FDA 승인 절차의 우선순위를 확보하게 된다. 또 향후 승인 과정에서 FDA와 빠르고 원활한 의사소통을 진행할 수 있다. 뿐만 아니라 유연한 임상 연구 설계, 전문 심사팀 배치 등 FDA의 긴밀한 지원을 받을 수 있다.
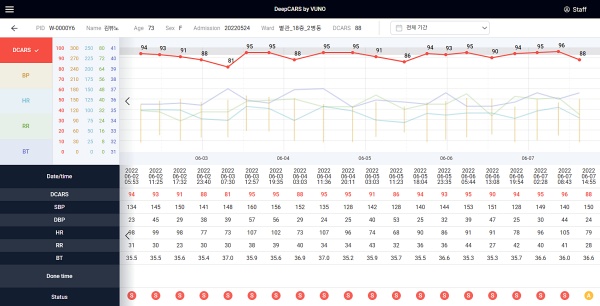
뷰노메드 딥카스는 일반병동에서 필수적으로 측정해 EMR(전자의무기록)에 입력하는 혈압, 맥박, 호흡, 체온 4가지 활력징후를 분석, 환자의 심정지 발생 위험도를 점수로 제공하는 AI 의료기기다.
이를 통해 모든 입원환자에 대한 상시 감시가 어려운 일반병동에서 의료진의 선제적 대응을 가능하게 한다. 확증 임상시험 연구 결과에 따르면 환자의 연령, 성별, 진료과 등 특정 제한사항 없이 유효성을 입증했다.
해당 제품은 입원환자의 생명을 위협하는 병원 내 심정지 발생에 대해 기존 중증악화 모니터링 도구 대비 획기적인 진단 기술로 환자에게 최선의 이익을 제공한다는 점 등을 인정받아 미국 FDA로부터 혁신의료기기로 지정됐다.
뷰노는 세계 최대 의료시장인 미국 보건당국의 공식 인정을 토대로 현지 시장 진출 준비에 속도를 올릴 계획이다.
현재 뷰노는 뷰노메드 딥카스의 미국 진출을 위해 현지 의료기관과 임상 연구를 수행하고 있으며 지난달 해당 제품 관련 핵심 기술에 대한 미국 특허 등록도 마쳤다.
이예하 대표는 “뷰노메드 딥카스는 뷰노의 생체신호 분야 주력 제품으로서 이번 FDA 혁신의료기기 지정으로 혁신성과 우수성을 다시 한번 입증했다”며 “국내에서 도입 병원이 꾸준히 증가하며 시장성을 입증하고 있는 상황에서 신속한 미국 FDA 승인을 준비하며 적극적인 현지 사전 마케팅을 추진하는 등 해외 매출 상승에 매진하겠다”고 밝혔다.

