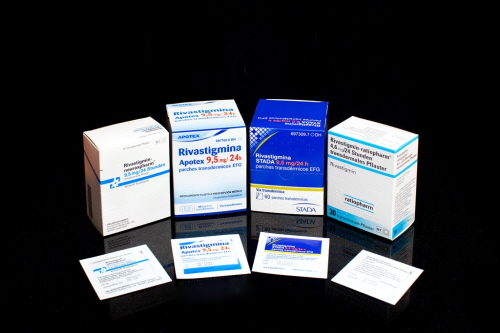
[라포르시안] SK케미칼은 자사 치매 치료 패치(SID710, 리바스티그민)’이 미국 식품의약국(FDA)로부터 최종 시판 허가를 받았다고 27일 밝혔다.
국내에서 개발된 치매치료 패치의 FDA 승인은 이번이 처음이다.
회사측에 따르면, SID 710은 SK케미칼이 국내 최초로 개발한 치매치료 패치다. 복약 시간과 횟수를 기억하기 힘들거나 알약을 삼키기 힘든 치매 환자들을 위해 하루 한 번 피부에 부착해 약물이 지속적으로 전달되도록 했다.
알약 형태의 경구용 제품과 효과는 같으면서 오심, 구토, 염증 등 부작용이 적고 위와 간에 부담이 적은 것이 장점으로 꼽힌다.
SID710의 이번 FDA 승인은 유럽(2013년), 호주(2016년), 캐나다(2018년) 진출에 이은 성과다. 지금까지 19개국에 진출, 24개 주요 제약사와 판권 및 수출 계약을 맺었다.
전광현 SK케미칼 사장은 “이번 FDA 승인을 통해 우리의 높은 기술력을 인정받았다. 글로벌 수준에 부합하는 개발 역량과 허가 대응 능력을 바탕으로 미국, 유럽에 이어 남미, 동남아시아 주요 국가들로 확대 진출할 예정”이라고 말했다.
한편 인구 노령화에 따라 전 세계 치매 치료제 시장은 확대되는 추세다.
글로벌 시장조사기관인 Data monitor healthcare에 따르면 2019년 현재 전 세계 치매환자 수는 230만 명에 달하며, 관련 치료제 시장은 연간 4조원(33억 달러) 규모로 추산됐다.
조필현 기자
chop23@rapportian.com
다른기사 
